【概述】
多年以來,ICP-MS一直是人體體液(尿液、血液、血清和唾液)以及組織和骨頭中鉛(Pb)、砷(As)、汞(Hg)和銅(Cu)等元素痕量分析的工具。單個元素,有毒或營養元素在*的基質中運行方式可為醫生提供關于患者的全面信息。近,由于植入物的普及,諸如鈦(Ti),鈷(Co)和釩(V)之類的元素已被添加到一般的測試分析列表中。
鈦(Ti)金屬被廣泛用于各種各樣的人體修復術,例如人工髖關節(圖1)、膝蓋、種植牙以及醫用夾子和螺釘等。人工關節實際上是由不同鈦合金制成,其中經常會混合少量鋁和釩。這些合金被稱為“醫用”鈦合金。在這個醫療領域中使用鈦有以下幾個原因。首先,由于鈦不受體液腐蝕,因此被視為具生物相容性的金屬,也是少數能夠整合入骨頭的金屬之一(骨整合)。此外,醫用鈦合金無毒,非磁性,具有與骨頭類似的靈活性和彈性。1

圖1.插圖顯示的是醫用鈦合金制成的置換用人工髖關節。
然而,由于人體髖部的球窩關節高強度的工作,鈦金屬會隨著時間流逝而慢慢磨損并進入血液。雖然鈦本身無毒,但是血液中的鈦含量水平能夠幫助醫療服務提供者了解植入體降解的程度。因此,監控植入人工髖關節的患者血清或髖關節抽出物中鈦含量十分重要。
但是由于種種因素限制(包括濃度低、眾多潛在的光譜干擾和復雜的人體體液基質)想要準確測量血清中的鈦含量比較困難。本研究將探索如何分析血清中的鈦含量,尋找有助于克服這種困難的儀器參數和方法。本實驗僅用于研究用途,不用作診斷評價。
【實驗/設備條件】
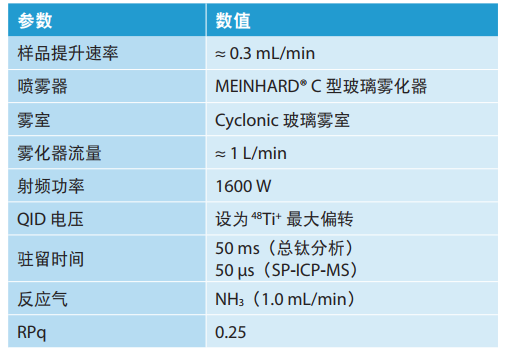
所有分析都在PerkinElmer NexION® 2000 ICP-MS上進行,分析條件如表1所示。由于鈦同位素存在諸多潛在干擾,因此分析過程中使用氨作為反應氣體,將鈦轉換為Ti-NH3簇/[TiNH(NH3)4](m/z 131)。為了將信號大化,四級桿離子偏轉器(QID)電壓設置用于傳輸m/z 48——豐富的鈦同位素(73.8%)。所有分析均在相似條件下使用相同的樣品導入成分,區別在于停留時間:總鈦測量使用的是50 ms停留時間,而SP-ICP-MS分析使用的是50 µs停留時間。將停留時間控制在低于100µs對于SP-ICP-MS分析而言十分關鍵,因為這樣有助于降低在相同分析時間窗內檢測到兩個納米顆粒的可能性。所有分析和數據處理均通過ICP-MS軟件的Syngistix™和Syngistix納米顆粒應用模塊來進行。
表1. NexION 2000 ICP-MS分析鈦含量儀器條件。
【實驗/操作方法】
本研究中使用的有證標準物質(CRM)為含有正常水平微量元素的血清(UTAK® Laboratories Inc., Valencia,California, USA)。此有證標準物質不是為鈦而認證,而是作為實驗中的血清基質。此外,患者樣品(血清和髖關節抽出物)來自University Hospital Saint-Louis -Lariboisière - Fernand-Widal, Paris, France。
在所有分析中,血清和抽出物均使用0.2% HNO3(Optima Grade, Thermo Fisher Scientic, Waltham,
Massachusetts, USA)稀釋20倍。稀硝酸能讓鈦在溶液中保持穩定,而保持低濃度有助于防止蛋白質和細胞碎片沉淀。總鈦分析時使用標準加入法(MSA),其中校準曲線的基質是稀釋了20倍的血清。而對于鈦納米微粒的分析,可行性試驗時使用的是NIST1898 TiO2納米微粒。NIST SRM 8013(60 nm金納米微粒)用于測定輸送效率(TE)。在稀釋20倍的血清中制備溶解態校準曲線。
【實驗結果/結論】
血清中總鈦測定
過往研究結果2顯示我們能夠在反應模式——質量轉移模式下變為氨團簇(m/z 131)的鈦進行測量。而在當前研究中,在優化NH3流速后(圖2),可以通過掃描確認是否存在Ti-NH3團簇(m/z 131)(圖3)。
在本研究中,QID電壓設為m/z 48大偏轉頻率(基于鈦大豐度同位素),而分析四極桿設為篩選m/z 131,即Ti-NH3團簇。通過QID電壓和四極桿的質量篩選,可以在分析反應產物時優化分析信號,同時去除潛在干擾。

圖2用于生成鈦團簇(m/z 131)的NH3流速優化(mL/min)。預計鈦檢出限(EDL)為1 ppt。

圖3.在130-132質量范圍內掃描Ti-NH3團簇。鈦濃度為1 ppb。
雖然氙也有m/z 130、131和132的同位素,但是氙能夠通過電荷轉移與NH3發生快速反應,因此在這些質量下只會余下極低cps的背景。樣品中總鈦分析使用標準加入法,標準曲線使用的20倍稀釋的UTAK血清中加入0.5、1和2 µg/L鈦標準溶液。圖4展示了曲線的相關系數為0.99996。

圖4. 20倍稀釋血清中的鈦標準加入法曲線(m/z 131)。
對三個樣品進行了分析:一個是血清標準物質(UTAK,沒有對鈦定值),另外兩個來自接受髖關節植入的患者——
其中一個為血清,另一個為髖關節抽出物(植入體周圍抽取的體液)。這三個樣品(稀釋20倍)的結果參見表2。UTAK(正常血清)標準物質中的鈦含量沒有標準值,但是結果較低,在20倍稀釋血清中估算檢出限大約為0.004 ug/L。
對UTAK血清中進行鈦加標0.5 µg/L,回收率為98%,證明此方法是準確的。患者樣品中的鈦含量更高,特別是在血清中。
表2. 20倍稀釋樣品中鈦分析結果。

接著,在三個樣品中分別加入1 µg/L TiO2納米顆粒(等同于0.6 µg/L鈦),并再次測定。表3所列結果顯示平均回收率為71%,但更值得注意的是RSD比沒有加標納米顆粒TiO2(表2)的血清樣品高出許多。這表明很可能血清鈦分析中觀察到的RSD升高是由于樣品中存在鈦納米顆粒。
表3.加入1 µg/L鈦納米顆粒到血清后鈦分析結果。

血清中鈦顆粒的單顆粒分析
為了確認能夠在m/z 131質量下能測定TiNH(NH3)4+鈦納米顆粒,我們對0.2% HNO3中的1 µg/L TiO2納米顆粒懸浮液進行分析。圖3顯示實時信號與時間曲線圖、粒徑與頻率柱狀圖,說明大概率粒徑為80 nm,與NIST認證中所示的71-83 nm非常接近。

圖5.以TiNH(NH3)4+(頂部)和對應的TiO2粒徑分布(底部)測量TiO2納米顆粒。
接著對UTAK有證標準物質血清、患者抽出物和患者血清進行Ti納米顆粒和溶解態鈦評估。
表4顯示UTAK血清三次獨立分析的SP-ICP-MS結果。其中就如同預計的標準物質一樣幾乎沒有檢測到鈦顆粒。此
結果與所有測量數據均保持一致。
表4. UTAK血清中鈦的SP-ICP-MS。

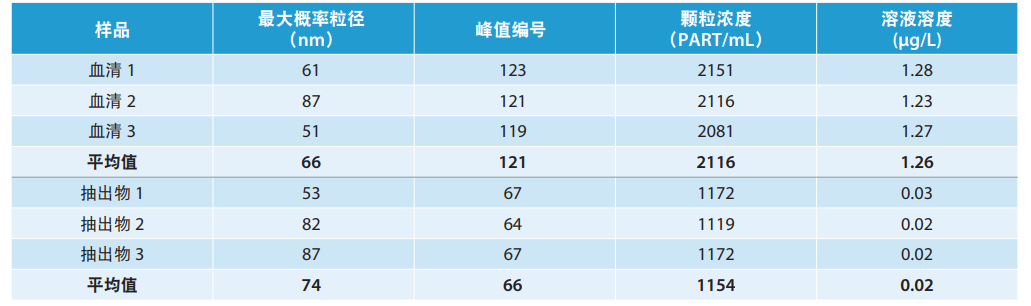
后分析取自患者人工髖關節的樣品。如表5所示,患者樣品中的顆粒遠遠高于標準物質,很可能是由于人工髖關節中鈦磨損所致。除此之外,患者血清中溶解鈦濃度與總鈦分析的測量結果十分相近。
表5.患者血清樣品的SP-ICP-MS結果。
結論
本研究證明我們能夠利用PerkinElmer NexION® 2000 ICP-MS的反應-質量轉移分析功能準確測量血清中低含量的鈦。通過將NH3作為反應池氣體,Ti+能夠反應形成TiNH(NH3)4+(m/z 131)來避免Ti+同位素的一般干擾。此外,事實證明該反應能夠有效測量血清中的鈦納米顆粒。綜合起來,這些結果表明鈦同時以溶解態和顆粒物狀態存在于取自患者人工髖關節的樣品中。但是還需要開展進一步研究以確定是否可以使用SP-ICP-MS進行植入體磨損的早期檢測,但是初步研究顯示這有很大希望。
立即詢價
您提交后,專屬客服將第一時間為您服務