【上海精瑞科學儀器有限公司 為 BIAseparations中國總代理 正規授權 售后無憂】一家專業提供HPLC色譜柱、GC色譜柱、SPE前處理小柱和其他實驗室常用耗材、配件的公司,同時提供各種進口標準品和各類分析儀器
:
156 0176 2218馮女士(vx同號)
QQ:3295336257
? AAV載體的應用現狀
基于腺相關病毒(AAV)的各種血清型載體被*在人類基因治療和基因疫苗接種應用中具有高潛力。在制造AAV載體期間,不必要的,不*的顆粒共同產生。它們缺乏重組病毒基因組,僅由空衣殼蛋白組成。空衣殼增加了用于醫學應用的AAV病毒的所需劑量,并且被認為引起針對載體衣殼的免疫反應,導致不必要的副作用。因此,在制造過程中去除空衣殼以及量化制劑中空AAV顆粒含量的能力是任何AAV生產過程的關鍵要求。
? 制備AAV載體的常規方法
目前用于制備分離空衣殼(CsCl或碘克沙醇梯度)的方法對于放大是具有挑戰性的并且不適合于大規模生產。此外,用于檢測空衣殼的分析方法和全空粒子比的測定(電子顯微鏡(EM)測定,總粒子測定[ELISA]結合基因組拷貝滴定[qPCR])耗費時間和勞動力,受操作者的影響技術或不提供用于不同血清型AAV的容易獲得的試劑。
?新突破
本應用簡報介紹了利用微小電荷差異分離全空和空AAV8顆粒的新方法。通過在BIA Seperations 的CIMmultus™ QA Monolithic column整體柱上使用線性梯度洗脫,引入了用于分析AAV顆粒的簡單,快速和可重復的分析。該方法成功應用于通過兩種不同制造工藝制備的AAV8顆粒。
材料與方法
通過CsCl梯度離心制備純化的完整和空AAV8載體顆粒的病毒制劑。
通過切向流過濾(TFF)然后通過碘克沙醇梯度進行AAV8的替代制備。
結果
電子顯微鏡
通過電子顯微鏡分析AAV8制劑制劑中*和空顆粒的存在。 空殼用箭頭表示(圖1)。
全衣殼和空殼AAV顆粒的色譜分離
用完整和空AAV8載體顆粒的CsCl梯度制備物進行初始結合 - 洗脫實驗。 線性鹽梯度下的不同保留體積表明可以對全載體和空載體顆粒進行色譜分離(數據未顯示)。
基于這些結果,將全粒子和空粒子的混合物應用于CIMmultus™ QA Monolithic column整體柱(圖2)。 將任意體積的75μL空衣殼制劑與1×10 12 GC的含有93.7%完整AAV載體顆粒(通過EM測量)的制劑混合(圖2)。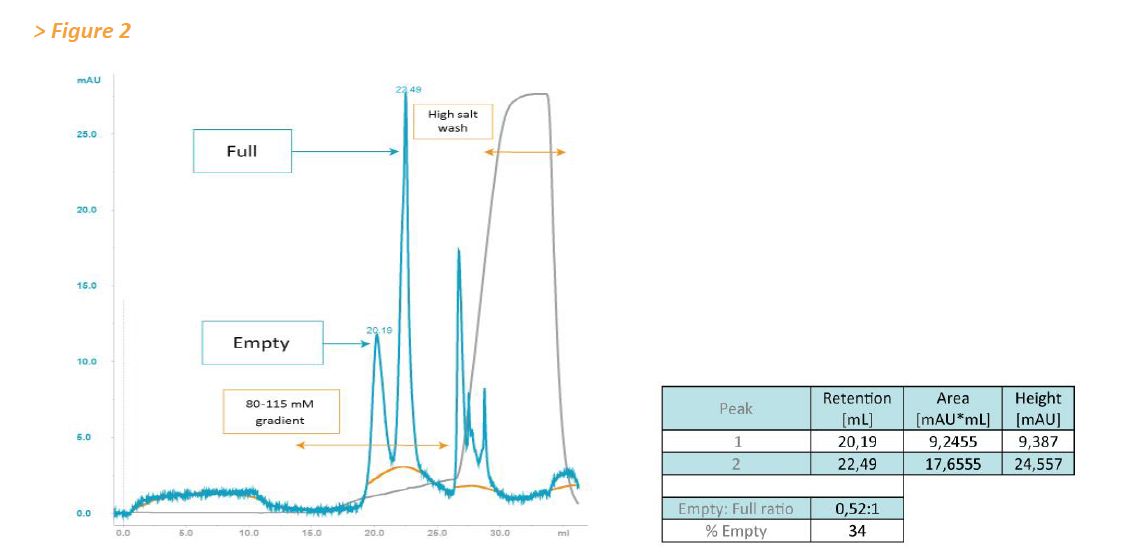
檢測到代表空衣殼和完整衣殼的明顯可區分的峰。 后來的洗脫峰含有> 99%的負載的全顆粒(通過qPCR測定)。 空衣殼的計算相對量(根據測量的峰面積)為34%(圖2)。
然后使用AAV8衣殼的色譜分離來分析不同AAV制劑中的全粒子與空粒子比率。 基于色譜峰積分,通過CsCl梯度(通過EM測量的93.7%飽和度)對AAV制劑的定量導致空 - 滿比率為0.016(1.6%空顆粒),而0.067(空顆粒為6.28%) 由EM分析確定(數據未顯示)。
通過替代方法產生的AAV顆粒的色譜分離和定量
接下來評估基于CIM QA的分離和定量的適用性,用于替代的AAV制備(通過TFF制備,隨后是碘克沙醇梯度)。 將含有相當于5×10 12 GC的AAV制劑加載到CIMmultus™ QA Monolithic column上,并用線性梯度洗脫分離,如色譜圖所示(圖3)。 與由CsCl制備的AAV相比,加載的AAV顆粒多5倍(圖2),這導致洗脫峰變寬。 在20.0分鐘洗脫的次要峰的峰面積與在22.2分鐘洗脫的主峰的積分(圖3)表明空 - 滿比為0.026(2.5%空顆粒),與EM獲得的比例很好地一致( 空 - 滿比率為0.05;空顆粒為4.5%)。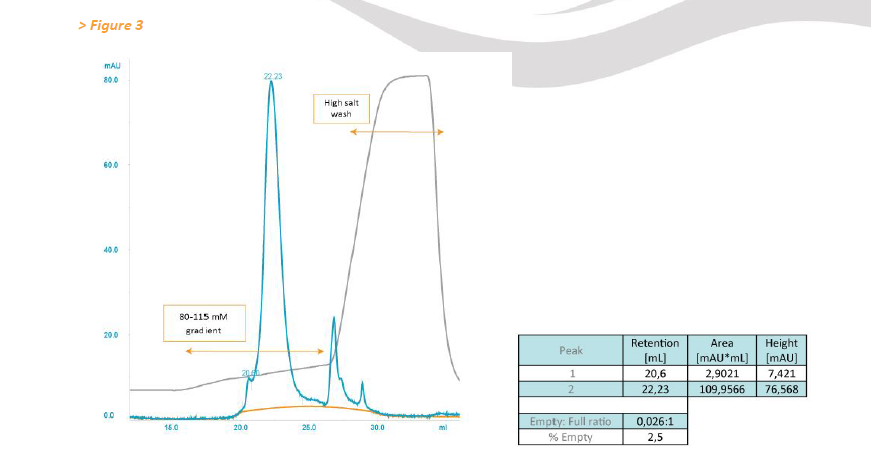
為了證明該方法對不同AAV生產過程的適用性,AAV樣品摻入空顆粒制劑,使用相同的梯度條件注入CIMmultus™ QA Monolithic column(圖4)。
分離和定量AAV顆粒(TFF和碘克沙醇梯度),加入空衣殼AAV
?結論:
開發了一種快速,可重復的方法,用于在CIMmultus™ QA Monolithic column上通過線性梯度洗脫分離和定量空顆粒和全顆粒AAV8載體。 該方案成功地用于兩種不同的AAV制劑,并且能夠定量空衣殼含量,這與替代方法一致。 色譜方法的優點是簡單,快速,不依賴于操作員技術和需要專門的試劑。 相反,它在單次測定中提供粒子特征的定量分析,運行時間為30分鐘。









 化工儀器網
化工儀器網