巴氏吸管由醫(yī)用級聚乙烯(PE)制成,管體
溶瘤病毒聯(lián)合CAR-T療法正當時,治療實體瘤如虎添翼
*,F(xiàn)DA已經(jīng)在2015年批準了溶瘤病毒療法T-VEC,用于不能手術的局部晚期或轉(zhuǎn)移性惡性黑色素瘤,這是一種攜帶重組粒細胞-巨噬細胞集落刺激因子(GM-CSF)的I型單純皰疹病毒病毒(HSV-1)。
然而,由于T-VEC的療效未盡如人意,其銷售情況與預期有一定的差距。為此,T-VEC正在黑色素瘤和其他實體惡性腫瘤的許多早期和晚期臨床試驗中進行組合療法的研究,包括與PD-1單抗(如Keytruda、Opdivo)、CTLA-4單抗(如Yervoy)等免疫檢查點抑制劑共同施用,以及與全身化療或放療的聯(lián)合,以求增強臨床療效和擴展適應癥。截至目前,已經(jīng)在幾個臨床試驗中發(fā)揮出不錯的效果,值得期待。
溶瘤病毒作為單一療法,仍存在不足
目前,溶瘤病毒(oncolytic virus, OV)作為癌癥患者的單一療法仍然存在許多絆腳石。
首先,OV可以全身給藥(靜脈注射)或瘤內(nèi)注射給藥,這兩種方法都與特定的優(yōu)點和缺點相關聯(lián):
- OV的全身給藥可以靶向的腫瘤細胞范圍更廣,但可能受到機體主動防御的限制:(1)機體通過中和抗體或通過循環(huán)內(nèi)的補體激活來隔離病毒顆粒;(2)其他障礙包括:異常腫瘤脈管系統(tǒng),非靶組織(可能被肺、肝或脾過濾)中的錯誤定位和隔離,以及循環(huán)中不充分的外滲,阻止其進入腫瘤微環(huán)境(TME)。
- OV局部滴注到腫瘤中可以繞過上述的許多障礙,T-VEC采用的正是此種給藥方法。然而,由于許多腫瘤位于體內(nèi)深處或靠近關鍵結構,對此進行局部給藥是不現(xiàn)實的。
就機制而言,OV可以選擇性地復制并殺死腫瘤細胞,并且由于腫瘤相關抗原(TAA)、病原體相關分子模式(PAMPS)和來自裂解的腫瘤細胞的危險相關分子模式(DAMPS)的釋放,OV可以刺激對腫瘤細胞的適應性免疫應答。這些反應也使得腫瘤由“冷”變“熱”,一旦被抗原呈遞細胞(APC)加工,TAA就可以與抗病毒反應同時誘導抗腫瘤T細胞應答。
此外,OV還能夠通過治療性轉(zhuǎn)基因的遞送,進一步增強宿主免疫細胞的抗腫瘤活性。
然而,由于溶瘤病毒存在免疫介導的作用機制,它需要相對完整的宿主先天和適應性免疫系統(tǒng),而這在癌癥患者中經(jīng)常受到損害。OV單一治療策略對病變的清除是不完整的,特別是對體積大和/或轉(zhuǎn)移的腫瘤,因此還需要額外的治療來增強其抗腫瘤作用。
CAR -T作為單一療法,同樣存在不足
在過去十年中,CAR -T細胞療法的臨床試驗數(shù)量不斷增多,達到了的研發(fā)熱潮,針對B細胞特異性細胞表面蛋白CD19的自體CAR-T細胞療法已經(jīng)成功誘導了難治性B細胞惡性腫瘤患者的持久和深度緩解,例如急性淋巴細胞白血病(ALL)或慢性淋巴細胞白血病(CLL)。
然而,目前尚無大規(guī)模有效的實體瘤CAR-T療法,其中的主要障礙包括:缺乏腫瘤特異性或抗原表達下調(diào);免疫抑制性腫瘤微環(huán)境缺乏必要的促炎刺激分子,并且含有豐富的抑制性檢查點分子;以及實體腫瘤塊的物理屏障。
這意味著,作為單一療法,CAR-T細胞不足以克服這些抑制機制,因此同樣需要額外的治療手段以增強其抗腫瘤作用。
溶瘤病毒與CAR-T細胞療法的聯(lián)合
CAR-T細胞療法的持久反應取決于供體T細胞的運輸和腫瘤中的存活,而OV可以重塑局部腫瘤微環(huán)境,改善T細胞募集和效應功能;對OV而言,與CAR-T細胞治療策略組合可以以互補和相加的方式起作用,克服OV對遠處(未治療)部位的有限抗腫瘤作用的局限性。
OV克服腫瘤微環(huán)境的免疫抑制

免疫抑制性腫瘤微環(huán)境
1- T細胞對致密/體積大的腫瘤可及性差;
2- 免疫抑制細胞的存在,如髓源抑制細胞(MDSC)和M2巨噬細胞;
3- MHC-I的表達下調(diào),導致抗原呈遞/識別不良;
4- 腫瘤細胞分泌趨化因子吸引免疫抑制細胞,如調(diào)節(jié)性T細胞(Treg);
5- 腫瘤細胞分泌抑制性細胞因子,如TGF-β、IL-10;
6- 腫瘤細胞通常缺乏可被內(nèi)源性T細胞識別的腫瘤特異性抗原;
7- 免疫檢查點分子(例如PD-L1)的表達導致T細胞衰竭。
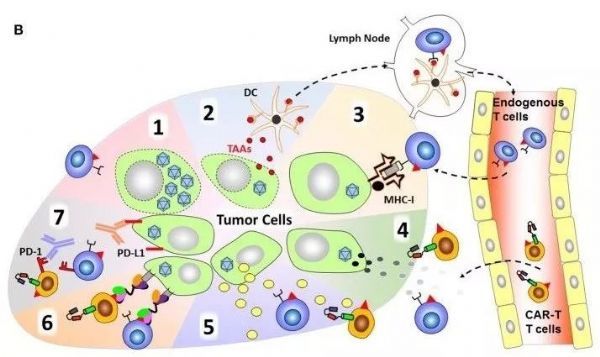
OV幫助T細胞克服免疫抑制性腫瘤微環(huán)境
1- OV通過直接對腫瘤細胞的直接裂解在腫瘤塊內(nèi)產(chǎn)生空間,增加腫瘤可及性;
2- 腫瘤細胞裂解后釋放DAMP、PAMP和TAA可以募集APC,并且TAA可將其呈遞給淋巴結處的T細胞;
3- OV感染可誘導MHC-I和β2M的表達;
4- 武裝OV表達趨化因子以增加內(nèi)源性T細胞和CAR-T細胞的浸潤;
5- 武裝OV表達炎性細胞因子以增加腫瘤部位的T細胞增殖;
6- 武裝OV表達雙特異性T細胞接合物(BiTE)分子以將T細胞重定向至腫瘤特異性抗原;
7- 武裝OV表達檢查點抑制劑以減輕T細胞衰竭。
臨床前研究已經(jīng)證明,上述組合治療策略可增強抗腫瘤活性。在黑色素瘤免疫活性小鼠模型中,研究人員證實溶瘤水皰性口炎病毒(oVSV)的瘤內(nèi)給藥促使腫瘤內(nèi)CD8 +T細胞的增加,與使用熱滅活的oVSV或未處理的小鼠(其中值存活期約為20天)的治療相比,觀察到T細胞浸潤并且30天內(nèi)存活率為50%。類似地,輸注OT-I(OVA特異性)T細胞在30天內(nèi)存活率為50%。
而當將oVSV治療與全身輸注OT-I T細胞相結合,50天時存活率約為70%,表明比單藥治療更有效的抗腫瘤反應。在類似的模型中,溶瘤腺病毒的瘤內(nèi)給藥與離體活化的OT-I T細胞結合使內(nèi)源性CD8 + T細胞的存在增加,促進腫瘤再激活的排斥。
這些結果證明:溶瘤性病毒療法與CAR-T細胞免疫療法相結合在免疫活性小鼠模型中是有益的,它們獨立地/附加地起作用以控制腫瘤生長。
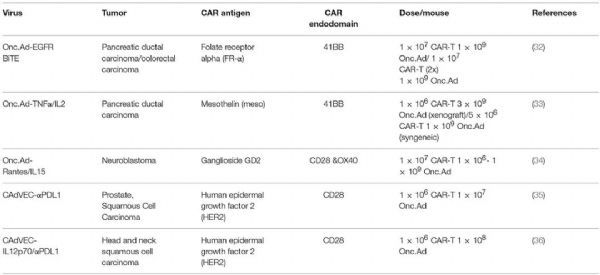
溶瘤病毒與CAR-T聯(lián)合的臨床前研究(圖片來源:frontier in immunology)
溶瘤病毒聯(lián)合CAR-T療法的潛在"武裝"策略
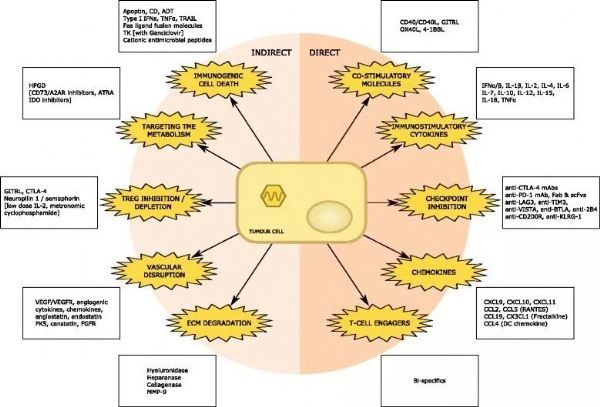
具有轉(zhuǎn)基因的重組溶瘤病毒賦予與CAR-T細胞療法的直接和間接協(xié)同作用
(圖片來源:BioMed)
重組基因工程的靈活性極大地促進了溶瘤病毒療法領域的復興,目前,許多“武裝”治療基因的OV正在進行臨床前和臨床研究。
例如,OV感染腫瘤有可能將細胞轉(zhuǎn)化為細胞因子和趨化因子工廠,從而將TME從免疫抑制轉(zhuǎn)變?yōu)樵试ST細胞進入和活化的免疫刺激環(huán)境。而這種潛力也創(chuàng)造了OV與CAR-T細胞療法發(fā)揮直接和間接協(xié)同作用的機會。
策略一 檢查點抑制劑
CAR-T細胞治療實體瘤的大障礙之一是腫瘤細胞上抑制性免疫檢查點配體的表達,包括CTLA-4、PD-1、B7-H家族成員和Fas配體。這些配體關閉效應T細胞功能,導致它們無法攻擊和控制腫瘤細胞。眾多臨床結果證明,靶向這些免疫檢查點分子的抗體可以有效地逆轉(zhuǎn)這種T細胞功能減退,然而這些抗體作為單一療法時僅對少部分患者適度有效。
同時,有證據(jù)表明OV治療期間PD-L1的表達增加,這可能是潛在的耐藥機制。為此,OV與PD-1/L1抗體的聯(lián)合療法正在進行廣泛的臨床試驗,并且取得了不俗的療效。正在進行的臨床前研究中,研究人員還探討了表達PD-1/CTLA-4抗體的CAR-T細胞/OV的療效。
上海交通大學基因治療專家蔡宇伽教授的基因治療公司本導基因也在溶瘤病毒方向有了重要突破,該公司將先進的基因編輯、合成生物學開關等生物學技術引入溶瘤病毒研發(fā)研發(fā)管線,使用與免疫檢查點技術聯(lián)合等核心技術以提高抗腫瘤療效。
策略二 雙特異性T細胞接合物(BiTE)分子
雙特異性T細胞接合物(BiTE)是由CD3-scFv組成的分子,可以將腫瘤駐留/浸潤的T細胞重定向至腫瘤細胞上表達的其他特異性抗原。盡管目前有許多BiTE分子正在開發(fā)用于臨床,但是可能需要解決全身和頻繁輸注導致的潛在副作用。
為此,OV已經(jīng)用于表達各種BiTE分子,可以增加BiTE分子的功效,并減少其全身給藥引起的副作用。腫瘤部位BiTE的局部組成型表達將為腫瘤駐留T細胞提供刺激,增加CAR-T細胞的浸潤和活化。
策略三 趨化因子/炎性細胞因子
T細胞在腫瘤部位發(fā)揮其細胞毒性作用之前,首先必須回到它們的目標并滲入腫瘤塊。趨化因子則是將免疫細胞吸引到炎癥部位的分子。
近證實,腫瘤內(nèi)給予溶瘤性II型單純皰疹病毒(HSV-2)可誘導多種促炎趨化因子(即CCL2、CCL3、CCL4、CXCL9、CXCL10、CXCL11)的高表達,從而增加內(nèi)源性T細胞和CAR-T細胞的浸潤和持久性。
抑制性腫瘤微環(huán)境耗盡了前T細胞細胞因子,這是腫瘤逃避細胞毒性T細胞的顯著抑制機制之一。OV可以通過遞送炎性細胞因子以刺激腫瘤部位的T細胞并逆轉(zhuǎn)這種無反應性,增加腫瘤部位的T細胞增殖。
結語
雖然腫瘤擅長創(chuàng)造免疫抑制微環(huán)境,但將OV與CAR-T細胞免疫治療相結合或許可以克服這些逃避機制。此外,基于目前部分有待改善的臨床試驗數(shù)據(jù),合理設計OV針對每種CAR構建體和每種靶腫瘤/組織的武裝基因,為特定腫瘤靶標提供T細胞*協(xié)同分子,或許能大化聯(lián)合治療的抗腫瘤效果。
兩種療法作為單一治療的安全性已在眾多臨床試驗中得到證實,在未來的實體腫瘤臨床試驗中,OV和CAR-T細胞療法的組合可能是更安全和更有效的治療方法。(生物谷)
參考出處:
DOI:10.1038/s41577-018-0014-6
DOI:10.3389/fimmu.2018.02103
DOI:10.1186/s40425-017-0294-6
 您好, 歡迎來到化工儀器網(wǎng)
您好, 歡迎來到化工儀器網(wǎng)

 11
11


